Erklärvideos rund um neuroonkologische Eingriffe
Glioblastom: Ursachen, Symptome und Therapie
Gliom: Ursachen, Symptome und Therapie
Hirnmetastasen Behandlung
Hirntumor-Diagnostik
Hirntumor: Ursachen, Symptome und Therapie
Komplementärmedizin
Literaturverzeichnis & Quellen
LITT und Immuntherapie
Personalisierte Impfungen
Schonende Hirntumor-Operationen
Tumorrezidivbehandlung
Schonende Hirntumor-OP – Funktion erhalten und maximal resezieren
Unser Ziel ist nicht die maximale Resektion um jeden Preis, sondern die schonende OP unter bestmöglichem Erhalt Ihrer Sprach-, Motorik- und kognitiven Funktionen.
Wir setzen auf ein multimodales Konzept modernster Techniken und innovativer Verfahren – jedes auf Ihre individuelle Situation abgestimmt. Hier informieren wir Sie im Detail:
Elektrisches Monitoring und Mapping für eloquente Areale
Durch elektrische Stimulation (Mapping) identifizieren wir funktionell kritische Areale in Echtzeit und schonen diese gezielt. Auf diese Operationstechniken sind wir spezialisiert.
Wenn die Funktionen, die wir besonders schützen müssen nicht durch eine Wachoperation überprüft werden müssen, können wir auch in einer durchgehenden Vollnarkose wichtige Gehirn- und Nervenfunktionen zu schützen – besonders wenn der Tumor in der Nähe von Arealen liegt, die für Bewegung und Gefühl verantwortlich sind. Wir nutzen dabei neurophysiologische Monitoring Techniken, um Risiken zu minimieren.
Inhaltsverzeichnis
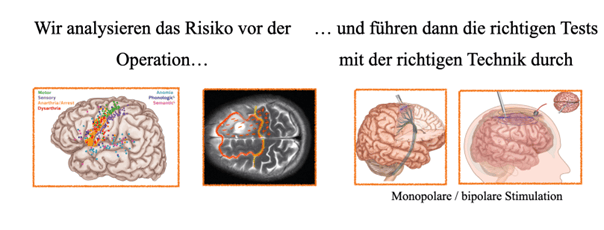
1. MEPs (Motorisch evozierte Potenziale): Monitoring
- Zweck: Überwachung der Bewegungsfunktionen.
- Wie es funktioniert: Über Elektroden am Kopf oder direkt am Gehirn werden schwache elektrische Impulse gegeben, die die motorischen Bahnen im Gehirn und Rückenmark aktivieren. Die Antwort wird in Muskeln (z. B. Hand oder Fuß) gemessen.
- Warum wichtig: Falls die Signalstärke abnimmt, warnt dies den Chirurgen vor einer möglichen Schädigung der Bewegungsareale.
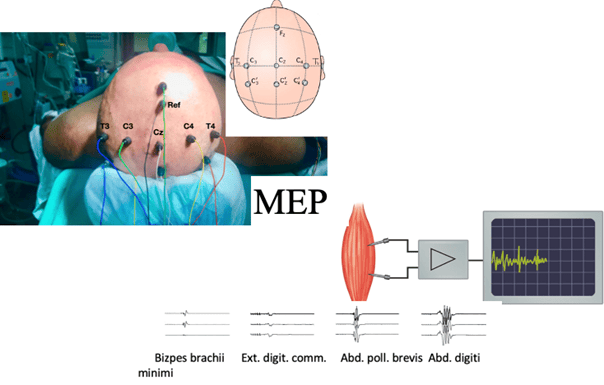
2. SSEPs (Somatosensibel evozierte Potenziale:Monitoring)
-
Zweck: Überwachung der Bewegungsfunktionen.
-
Wie es funktioniert: Über Elektroden am Kopf oder direkt am Gehirn werden schwache elektrische Impulse gegeben, die die motorischen Bahnen im Gehirn und Rückenmark aktivieren. Die Antwort wird in Muskeln (z. B. Hand oder Fuß) gemessen.
-
Warum wichtig: Falls die Signalstärke abnimmt, warnt dies den Chirurgen vor einer möglichen Schädigung der Bewegungsareale.
3. Monopolare Stimulation (Direkte kortikale/subkortikale Stimulation)
-
Zweck: Präzise Identifikation von funktionell wichtigen Arealen während der Operation.
-
Wie es funktioniert: wir stimulieren mit einer feinen Sonde direkt das Gehirngewebe um den Tumor. Bei Stimulation motorischer Regionen zuckt z. B. der entsprechende Muskel des Patienten (in Narkose überwacht).
-
Warum wichtig: So können Regionen die Bewegungsfunktionen steuern geschont werden. Dabei gehen wir systematisch die Oberfläche oder in der Tiefe die Tumorhöhle ab und erstellen eine Karte der Bewegungsfunktionen (Mapping).
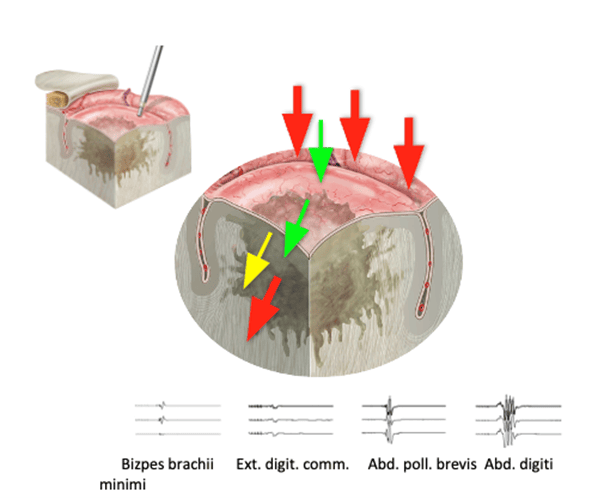
Zusammenfassung Mapping und Monitoring
Diese Methoden arbeiten wie ein „Echtzeit-Überwachungssystem“ für das Gehirn:
- MEP/SSEP = Globale, kontinuierliche Überwachung der Nervenbahnen (Monitoring)
- Monopolare Stimulation = Erkennen der lokalen Bewegungsfunktionen des Gewebes (Mapping).
Dank dieser Techniken wir den Tumor möglichst vollständig entfernen, während wichtige Funktionen erhalten bleiben.

„Die Durchführung von Wachoperationen gehört zu unserer Kernkompetenz. Insgesamt haben wir bereits mehr als 1.000 Wachoperationen durchgeführt und gehören damit zu den erfahrensten Operateuren, die diese Technik anwenden.
Eine Wachoperation mag ungewöhnlich klingen, doch sie ist ein bewährtes Verfahren, um Ihr Gehirn zu schützen. Wir werden Sie sehr eng begleiten – fragen Sie vorher gerne alles, was Ihnen wichtig ist.
Ihre Gesundheit steht im Mittelpunkt: Mit dieser Methode können wir gezielt handeln, um Ihre Lebensqualität zu erhalten.“
– Prof Dr. med. Marion Rapp
Vertrauen Sie auf eines der erfahrensten Teams Deutschlands für Hirntumor-Wachoperationen
Wir begleiten Sie einfühlsam und auf Augenhöhe – von der Vorbereitung bis zur sicheren Entfernung des Tumors.
Ihr Spezialisten-Team für komplexe Hirntumor-Operationen – Erfahrung, die den Unterschied macht
Sie suchen Spezialisten für eine Hirntumor-OP, bei der mehr zählt als das bloße Entfernen eines Tumors?
In der Beta Klinik verbinden wir langjährige neurochirurgische Erfahrung mit Methoden wie der Wachkraniotomie, um lebenswichtige Funktionen gezielt zu schützen.
Wachoperation bei Hinrntumoren
Bei Tumoren in sprach- oder motorisch wichtigen Regionen (eloquente Areale) führen wir Wachoperationen durch. Sie sind während der OP wach, damit wir Ihre Sprach- und Motorikfunktionen kontinuierlich testen können.
Die Durchführung von Wachoperationen gehört zu unserer Kernkompetenz. Insgesamt haben wir bereits mehr als 1000 Wachoperationen durchgeführt und gehören damit zu den erfahrensten Operateuren, die diese Technik anwenden.
Wachoperationen bei Hirntumoren – Was Sie wissen sollten
Hirntumor-Operationen klingen oft beängstigend, besonders wenn Sie hören, dass Sie dabei wach sein sollen. Doch diese Methode (auch „Wachkraniotomie“ genannt) wird eingesetzt, um Ihr Gehirn während der OP bestmöglich zu schützen.
Warum wird eine Wachoperation durchgeführt?

„Manche Hirntumore liegen nah an Bereichen, die für wichtige Fähigkeiten wie Sprechen, Bewegen oder Sehen zuständig sind. Einige dieser Fähigkeiten, insbesondere die Sprache, können nur im Wachzustand geprüft werden. Um diese wichtigen Funktionen zu schützen, betäuben wir das Gewebe rund um den Tumor kurzzeitig mithilfe elektrischer Impulse. So können wir genau feststellen, ob der betroffene Bereich sicher entfernt werden kann – oder ob er erhalten bleiben muss, um z. B. Ihre Sprache zu bewahren.
Dies Wachoperation erlaubt es uns, Tumorgewebe maximal sicher zu entfernen, ohne gesunde, funktionstragende Bereiche zu verletzen. Und das Wichtigste: Sie spüren dabei keine Schmerzen – höchstens ein leichtes Druckgefühl.“
– Prof Dr. med. Michael Sabel
Ablauf der Wach-OP: Schritt-für-Schritt erklärt
Vor der OP besprechen wir mit Ihnen sehr genau, was Sie erwartet. Das ist sehr wichtig, da Sie entspannt und vertrauensvoll in die OP gehen sollen. Wir nehmen uns viel Zeit. Sie sind ein Teil des Behandlungsteams und wir besprechen gemeinsam welche Ziele wir uns für die Operation setzen. Unser Team hat sehr fortschrittliche Tests entwickelt, die besser als die herkömmlich genutzten Tests Ihre Sprach- und Bewegungsfunktionen überprüfen. Diese Tests werden individuell angepasst und vor der Operation geübt.
Zu Beginn der OP schlafen Sie unter Vollnarkose. Am Anfang der Schlafphase wird die Kopfhaut lokal betäubt, so dass Sie im weiteren Verlauf der OP keine Schmerzen spüren. In dieser Phase öffnen wir behutsam den Schädelknochen, eröffnen die Hirnhaut und führen vorbereitende Tests durch
Sobald wir diese Vorbereitung abgeschlossen haben, werden Sie sanft geweckt. Nun testen wir gezielt Ihre Hirnfunktionen, indem wir die vorbereiteten Tests durchführen.
- Wir bitten Sie z.B., Fragen zu beantworten, Bilder zu benennen oder Finger/Hände zu bewegen.
- Gleichzeitig stimulieren wir bestimmte Hirnareale, um „sichere Zonen“ für die Tumor-Entfernung zu finden. Es ist gewollt, dass Sie zwischenzeitlich für wenige Sekunden „Ausfälle“ haben: wir erklären Ihnen das dann alles sehr genau während der OP.
- Sie spüren in dieser Phase keine Schmerzen – höchstens ein leichtes Druckgefühl.
Nach der Tumor-Entfernung schlafen Sie wieder ein. Der Schädel wird verschlossen, und die Wunde vernäht.
- Präzision: Geringeres Risiko, gesunde Hirnbereiche zu verletzen.
- Sofortige Kontrolle: Funktionen wie Sprache lassen sich direkt während der OP überprüfen.
- Kürzere Erholung: Da weniger Gewebe geschädigt wird, ist die Rehabilitation oft einfacher.

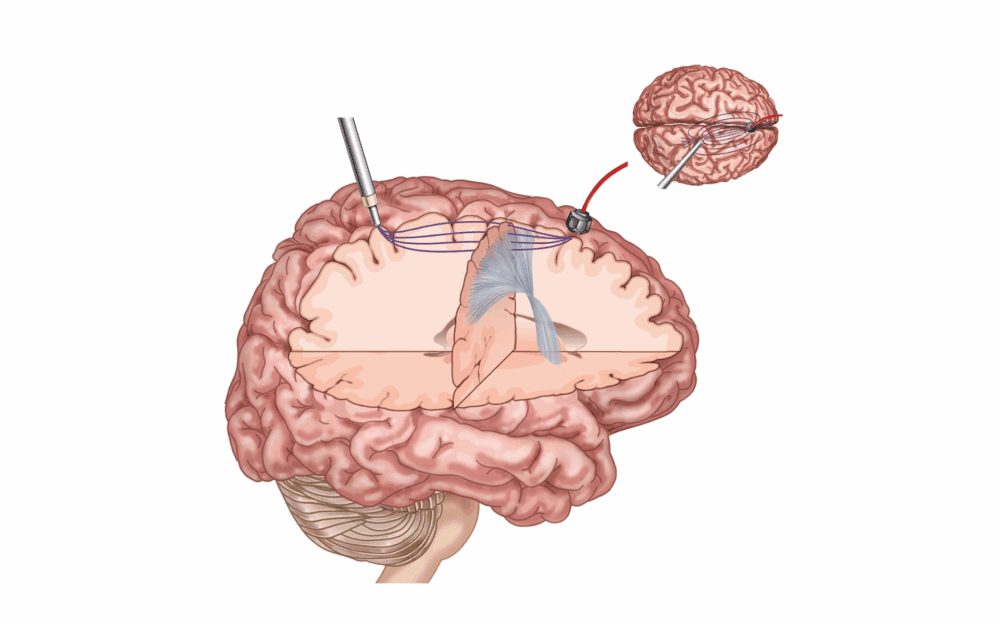
Was passiert nach der Wach-OP am Gehirn?
Sie werden nach der Operation durch unser Anästhesieteam intensiv überwacht und in der Folge auf unserer spezialisierten Station weiterbetreut. Wenn Sie es wünschen, dürfen Sie jetzt schon Besuch empfangen.
- Mögliche Nebenwirkungen wie Kopfschmerzen oder Müdigkeit klingen meist nach einigen Tagen ab.
- Durch die Nähe der Gewebsentfernung zu Bewegungs- Sprach -oder Gefühlsarealen kann es zu vorübergehenden Störungen dieser Funktionen kommen: das Gewebe ist „etwas beleidigt“ und erholt sich schnell.
- Logopädie oder Physiotherapie werden Ihnen helfen, eingeschränkte Fähigkeiten schneller wiederzuerlangen
- Sehr selten treten trotz aller Vorsichtsmaßnahmen bleibende Schäden auf. Es ist sehr wichtig, dass Sie dies verstehen und sich bewusst auf dieses Risiko einlassen. Wir erklären Ihnen sehr genau, warum wir Ihnen dieses „Restrisiko“ zumuten wollen.
Wertvolle Kombination mit Immuntherapie
Immuntherapien wie Checkpoint-Hemmer aktivieren die körpereigene Abwehr, stoßen bei Hirntumoren jedoch an Grenzen: Die Blut-Hirn-Schranke und das immunsuppressive Tumormilieu erschweren ihre Wirkung.
Die Laserthermotherapie (LITT) kann hier unterstützen. Durch die Hitzeeinwirkung werden Tumorzellen zerstört und Antigene freigesetzt, die eine Immunantwort anregen – ähnlich einem „Impfstoff-Effekt“. Zudem öffnet die LITT vorübergehend die Blut-Hirn-Schranke, wodurch Immuntherapeutika wirksamer werden können. Erste Studien deuten darauf hin, dass die Kombination Tumorkontrolle und Ansprechen auf die Behandlung verbessert.
An der Beta Klinik nutzen wir diesen Ansatz vor allem bei Gliomen wie dem rezidivierenden Glioblastom sowie bei Hirnmetastasen, etwa von Melanomen oder Lungenkarzinomen. Geeignet ist die Kombination insbesondere dann, wenn eine Operation riskant wäre oder bereits eine Immuntherapie Wirkung zeigt. Nach interdisziplinärer Bewertung erfolgt gegebenenfalls zunächst die LITT, anschließend eine individuell angepasste Immuntherapie mit engmaschigem MRT- und Labor-Monitoring.
So eröffnet die Kombination neue Chancen für eine personalisierte Behandlung, insbesondere bei aggressiven oder wiederkehrenden Hirntumoren. Wir beraten Sie gerne, ob dieses Verfahren in Ihrem Fall sinnvoll ist. Wir klären Sie transparent über alle Optionen auf und unterstützen Sie bei der Entscheidung. Ihr Wohlbefinden und der Erhalt Ihrer Lebensqualität stehen im Mittelpunkt.
Verschiedene Tumorarten – individuelle OP-Konzepte
Zentrum für Hirntumore an der Beta Klinik Bonn

Wir begleiten Sie und Ihr Leben auch nach der Hirntumor-OP
Eine erfolgreiche Operation des Hirntumors ist nur der erste Schritt. In der Beta Klinik Bonn endet die Versorgung nicht im OP-Saal: Unser interdisziplinäres Team unterstützt Sie auch danach – mit gezielter Rehabilitation, Logopädie, neurokognitivem Training und psychoonkologischer Begleitung. Denn es geht nicht nur um Heilung, sondern darum, Ihr Leben aktiv und selbstbestimmt fortzusetzen.
Ihre Vorteile bei einer Wachoperation – Sicherheit durch Präzision
Eine Wachoperation mag auf den ersten Blick ungewöhnlich wirken – doch sie ist ein seit vielen Jahren bewährtes Verfahren, um das Gehirn bei einer Hirntumor-OP gezielt zu schützen. Prof. Dr. med. Michael Sabel und Prof. Dr. med. Marion Rapp zählen zu den erfahrensten Operateuren auf diesem Gebiet und begleiten Sie einfühlsam durch alle Phasen des Eingriffs.
Sie möchten prüfen lassen, ob eine Hirntumor-OP in Ihrem Fall sinnvoll und sicher möglich ist? Nutzen Sie einfach unseren digitalen Weg:
- Formular ausfüllen: Datenschutzerklärung und Kostenübernahme bestätigen.
- Befunde hochladen: z. B. MRT-/CT-Bilder, OP-Berichte, Arztbriefe und/oder Selbstbewertungsbögen.
- OP-Einschätzung erhalten: Unsere Spezialisten bewerten Ihren Fall und geben eine fundierte Empfehlung.
- Die Beratung ist häufig in einem ersten Schritt als Online-Meeting sinnvoll, auch um erste offene Fragen klären. Wenn wir Diagnostik und Therapie empfehlen, erhalten Sie schnell einen Präsenztermin.
Die Wachoperation zählt zu den sichersten Verfahren der modernen Neurochirurgie, wenn es darum geht, wichtige Hirnfunktionen wie Sprache oder Bewegung zu schützen. Für Patientinnen und Patienten bedeutet das: mehr Kontrolle, mehr Sicherheit – und oft eine schnellere Erholung.
Zum Abschluss
Eine Wachoperation mag ungewöhnlich klingen, doch sie ist ein bewährtes Verfahren, um Ihr Gehirn zu schützen. Wir werden Sie sehr eng begleiten – fragen Sie vorher gerne alles, was Ihnen wichtig ist.
Ihre Gesundheit steht im Mittelpunkt: Mit dieser Methode können wir gezielt handeln, um Ihre Lebensqualität zu erhalten.
Innovative Sprachtestung nach Prof. Grodzinsky
In Zusammenarbeit mit einem führenden Sprachwissenschaftler – Prof. Grodzinsky von der Hebrew University Jerusalem – haben wir innovative Testverfahren entwickelt.
Diese erfassen die Sprachfunktion deutlich besser als herkömmliche Testungen. Diese Erkenntnisse sind von uns in einer Fachzeitschrift veröffentlicht worden:
(Rapp, Sabel, Grodzinsky 2026 (hier gehts zur Publikation).
Yosef Grodzinsky ist derzeit Direktor des Neurolinguistik-Labors am Edmond and Lily Safra Center for Brain Sciences und Professor Emeritus an der Hebräischen Universität Jerusalem. Außerdem ist er wissenschaftlicher Mitarbeiter am Institute for Neuroscience
and Medicine, Forschungszentrum Jülich, sowie am Cécile und Oskar Vogt Institut für Hirnforschung am Universitätsklinikum Düsseldorf.
Er ist Träger eines Alexander-von-Humboldt-Preises und war zuvor Inhaber des Canada Research Chair (Senior Chair) für Neurolinguistik an den Departments für Linguistik und Neurologie/Neurochirurgie der McGill University.
Neurokognitive Untersuchung vor und nach OP
Gemeinsam mit unseren Neuropsychologen identifizieren wir auch häufig nicht untersuchte neurokognitive Einschränkungen – vor und nach der Operation – und unterstützen Sie gezielt. Dazu nutzen wir etablierte Diagnostik- und Trainingsmethoden wie z.B. die Neuronation App.
Fluoreszenzgestützte Operation
Mit fluoreszierenden Farbstoffen lässt sich Tumorgewebe während der OP leuchtend darstellen – gesundes Hirngewebe bleibt dunkel. Das erhöht die Sicherheit und schützt funktionell wichtige Areale.
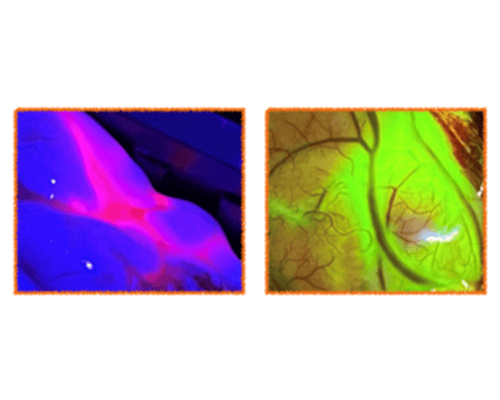
5-ALA Fluoreszenz bei Gliomen
5-ALA wird vor der Operation eingenommen und reichert sich spezifisch in Gliom-Gewebe an. Unter speziellem Licht beginnt der Tumor rot zu leuchten – so können wir ihn vollständiger entfernen.

Fluoreszin bei Hirnmetastasen
Fluoreszin ist ein Farbstoff, der spezifisch Metastasen anfärbt und ihre vollständige Resektion ermöglicht. Die Fluoreszenz ist intensiver als bei herkömmlichen Verfahren.
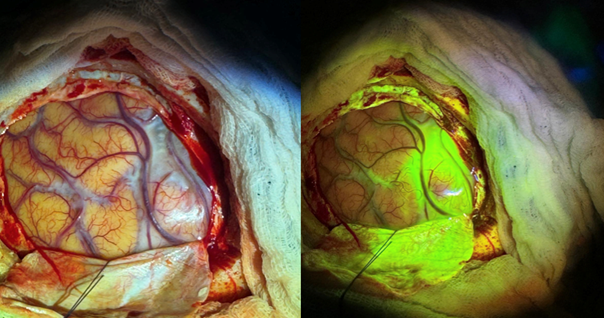
HLLS-Kopfleuchten-System – überlegene Technologie
Unsere Arbeitsgruppe hat kürzlich in einer wissenschaftlichen Arbeit nachgewiesen, dass unser Kopfleuchten-Lupen-System (HLLS) der konventionellen Mikroskop-Technologie deutlich überlegen ist – mit intensiverer Fluoreszenz und besserer Visualisierung der Tumorinfiltrationszone (Sabel, (...), Rapp, World Neurosurgery, 2025) . Das bedeutet für Sie: vollständigere Resektion bei besserem Erhalt gesunden Gewebes.

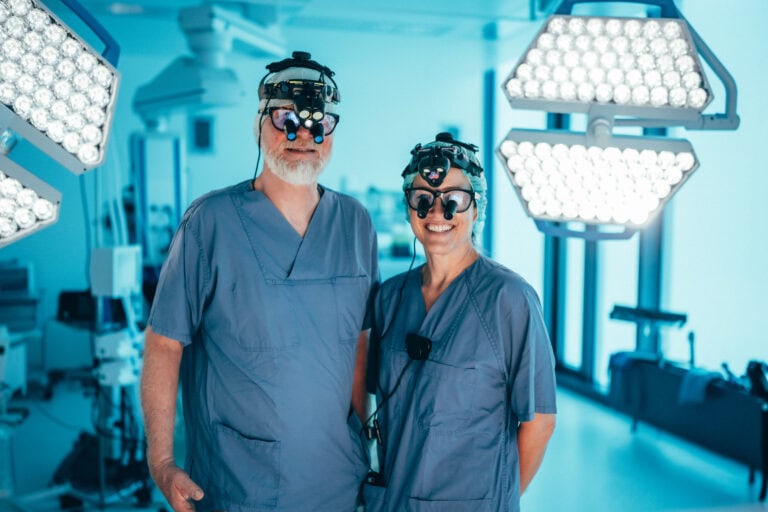
FET-PET-navigierte Chirurgie: die entscheidende Information
Die FET-PET misst die Stoffwechselaktivität des Tumors und unterscheidet zuverlässig zwischen echtem Tumorrezidiv und behandlungsbedingten Veränderungen (z. B. Strahlennekrosen). Wir integrieren diese Informationen direkt in unsere OP-Planung und steuern die verdächtigen Areale mit einem neuartigen Navigationsverfahren gezielt an.
Entscheidend für moderne Immuntherapien: Durch diese gezielte Biopsie gewinnen wir optimales Biomaterial aus den biologisch relevantesten Tumoranteilen – die Grundlage für personalisierte Impfungen gegen Hirntumore (z. B. Peptid-Vakzine oder dendritische Zelltherapie) sowie für die Identifikation von zielgerichteten Therapieoptionen.
Das bedeutet für Sie: präzise Diagnostik, bessere Therapieentscheidungen und Zugang zu innovativen Behandlungen.
Metabolische Bildgebung direkt in OP-Navigation
Wir gehören zu den wenigen Zentren in Deutschland, die FET-PET-Informationen direkt in die Navigation einlesen und intraoperativ nutzen können.
Die Areale mit erhöhtem Stoffwechsel werden in unser Neuronavigationssystem importiert und mit der MRT fusioniert. So können wir während der Operation gezielt die biologisch relevantesten Tumoranteile ansteuern.
Häufige Fragen und Sorgen - unsere Antworten
Nein. Das Gehirn hat keine Schmerzrezeptoren. Dank lokaler Betäubung und Narkose spüren Sie in der Regel nur ein leichtes Druckgefühl. Sollten wider Erwarten doch Schmerzen auftreten, können diese jederzeit schnell und zuverlässig gestillt werden.
Sie sind nicht allein. Wir begleiten Sie aktiv durch die OP. Sollte es doch zu Überforderung kommen, können wir Sie jederzeit wieder in Vollnarkose versetzen.
Die Überlebenschancen nach einer Hirntumor-OP hängen von vielen Faktoren ab: Tumorart, Lage, allgemeinem Gesundheitszustand und Therapiekombination.
Bei langsam wachsenden (niedriggradigen) Gliomen können Jahrzehnte guter Lebensqualität gewonnen werden. Wir sehen nun auch Patienten mit praktisch normaler Lebenserwartung, trotz der Diagnose eines niedriggradigen Glioms. Und auch bei den schnellwachsenden Gliomen sehen wir nun immer mehr Patienten, die als „Langzeitüberleber“ viele Jahre mit guter Lebensqualität gewinnen können.
Alle diese Patienten haben (oft trotz ungünstiger Genetik) eins gemeinsam: Sie haben den Kampf aufgenommen und die möglichen Therapien durchgeführt und durchgehalten.
Wie bei jedem Eingriff kann es auch bei der Hirntumor-OP zu Komplikationen wie Blutungen, Infektionen oder vorübergehenden Ausfällen von Sprache oder Bewegung kommen. In der Beta Klinik setzen unsere erfahrenen Neurochirurgen modernste Verfahren ein, um solche Risiken so gering wie möglich zu halten.
Ein Hirntumor gilt als inoperabel, wenn er so liegt, dass eine Entfernung zu große Risiken für wichtige Funktionen wie Sprache oder Bewegung bergen würde. Auch in solchen Fällen prüfen wir an der Beta Klinik alternative Behandlungswege wie Strahlentherapie, Immuntherapie oder Studienzugänge individuell. Oft finden wir Lösungen, auch wenn Ihnen gesagt wurde, dass nichts mehr geht. Es kommt immer auf den Einzelfall an.
Die meisten Patient:innen sind durch die Beruhigungsmittel entspannt. Wir leiten Sie durch jede Aufgabe und sorgen für Sicherheit.
Ihre Vorteile in der Beta Klinik – Privates Facharzt- und Klinikzentrum in Bonn
Literaturstellen
Hier finden Sie die wissenschaftlichen Fachartikel, die das Fundament unserer Arbeit sind. Alle Arbeiten sind in anerkannten wissenschaftlichen Journalen nach dem sogenannten Peer-review Verfahren veröffentlicht, entsprechen also dem höchsten wissenschaftlichen Standard. Fast alle dieser Arbeiten sind öffentlich zugänglich. Wollen Sie mehr erfahren, kopieren Sie die Literaturstelle in Ihren Browser und Sie finden die Originalarbeit.
- Herrlinger U, Schafer N, Steinbach JP, et al. Bevacizumab Plus Irinotecan Versus Temozolomide in Newly Diagnosed O6-Methylguanine-DNA Methyltransferase Nonmethylated Glioblastoma: The Randomized GLARIUS Trial. J Clin Oncol. May 10 2016;34(14):1611-9. doi:10.1200/JCO.2015.63.4691
- Herrlinger U, Tzaridis T, Mack F, et al. Lomustine-temozolomide combination therapy versus standard temozolomide therapy in patients with newly diagnosed glioblastoma with methylated MGMT promoter (CeTeG/NOA-09): a randomised, open-label, phase 3 trial. Lancet. Feb 16 2019;393(10172):678-688. doi:10.1016/S0140-6736(18)31791-4
- Schafer N, Proescholdt M, Steinbach JP, et al. Quality of life in the GLARIUS trial randomizing bevacizumab/irinotecan versus temozolomide in newly diagnosed, MGMT-nonmethylated glioblastoma. Neuro Oncol. Jun 18 2018;20(7):975-985. doi:10.1093/neuonc/nox204
- Tzaridis T, Schafer N, Weller J, et al. MGMT promoter methylation analysis for allocating combined CCNU/TMZ chemotherapy: Lessons learned from the CeTeG/NOA-09 trial. Int J Cancer. Apr 1 2021;148(7):1695-1707. doi:10.1002/ijc.33363
- Weller M, Tabatabai G, Kastner B, et al. MGMT Promoter Methylation Is a Strong Prognostic Biomarker for Benefit from Dose-Intensified Temozolomide Rechallenge in Progressive Glioblastoma: The DIRECTOR Trial. Clin Cancer Res. May 1 2015;21(9):2057-64. doi:10.1158/1078-0432.CCR-14-2737
- Wick A, Kessler T, Platten M, et al. Superiority of temozolomide over radiotherapy for elderly patients with RTK II methylation class, MGMT promoter methylated malignant astrocytoma. Neuro Oncol. Aug 17 2020;22(8):1162-1172. doi:10.1093/neuonc/noaa033
- Zeyen T, Potthoff AL, Nemeth R, et al. Phase I/II trial of meclofenamate in progressive MGMT-methylated glioblastoma under temozolomide second-line therapy-the MecMeth/NOA-24 trial. Trials. Jan 19 2022;23(1):57. doi:10.1186/s13063-021-05977-0
- Wick W, Roth P, Hartmann C, et al. Long-term analysis of the NOA-04 randomized phase III trial of sequential radiochemotherapy of anaplastic glioma with PCV or temozolomide. Neuro Oncol. Nov 2016;18(11):1529-1537. doi:10.1093/neuonc/now133
- Sabel M, Staub-Bartelt F, Todter J, et al. Improved Availability of Fluorescence-Guided Surgery of Malignant Brain Tumors: A Headlamp-Loupe System Combined With Generic 5-Aminolevulinic Acid Replaces the Microscope-A Monocentric Feasibility Study. World Neurosurg. Jun 2025;198:123967. doi:10.1016/j.wneu.2025.123967
- Campian JL, Le SB, Ghiaseddin A, et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun. Feb 26 2026;17(1)doi:10.1038/s41467-026-69522-w
- Latzer P, Zelba H, Battke F, et al. A real-world observation of patients with glioblastoma treated with a personalized peptide vaccine. Nat Commun. Aug 11 2024;15(1):6870. doi:10.1038/s41467-024-51315-8
- Rapp M, Grauer OM, Kamp M, et al. A randomized controlled phase II trial of vaccination with lysate-loaded, mature dendritic cells integrated into standard radiochemotherapy of newly diagnosed glioblastoma (GlioVax): study protocol for a randomized controlled trial. Trials. May 25 2018;19(1):293. doi:10.1186/s13063-018-2659-7
- Liau LM, Ashkan K, Brem S, et al. Association of Autologous Tumor Lysate-Loaded Dendritic Cell Vaccination With Extension of Survival Among Patients With Newly Diagnosed and Recurrent Glioblastoma: A Phase 3 Prospective Externally Controlled Cohort Trial. JAMA Oncol. Jan 1 2023;9(1):112-121. doi:10.1001/jamaoncol.2022.5370
- Galldiks N, Stoffels G, Filss C, et al. The use of dynamic O-(2-18F-fluoroethyl)-l-tyrosine PET in the diagnosis of patients with progressive and recurrent glioma. Neuro Oncol. Sep 2015;17(9):1293-300. doi:10.1093/neuonc/nov088
- Satish S, Athavale M, Kharkar PS. Targeted therapies for Glioblastoma multiforme (GBM): State-of-the-art and future prospects. Drug Dev Res. Nov 2024;85(7):e22261. doi:10.1002/ddr.22261
- Bonucci M, Fuggetta MP, Anelli L, Giannarelli D, Fiorentini C, Ravagnan G. New Approach for Enhancing Survival in Glioblastoma Patients: A Longitudinal Pilot Study on Integrative Oncology. Cancers (Basel). Jul 12 2025;17(14)doi:10.3390/cancers17142321
- Duffau H. A series of 309 awake surgeries with transcortical approach for IDH-mutant low-grade glioma involving the insula: long-term onco-functional outcomes in 253 consecutive patients. J Neurosurg. Sep 1 2025;143(3):765-772. doi:10.3171/2025.1.JNS242462
- Staub-Bartelt F, Rapp M, Sabel M. Feasibility of intraoperative neuromonitoring and cortical/subcortical mapping in patients with cerebral lesions of highly functional localizations-pathway to case adapted monitoring and mapping procedures. Front Oncol. 2023;13:1235212. doi:10.3389/fonc.2023.1235212
- Staub-Bartelt F, Rapp M, Sabel M. Resection of Eloquent Located Brain Tumors by Mapping Only-A Feasibility Study. Brain Sci. Sep 25 2023;13(10)doi:10.3390/brainsci13101366
- Staub-Bartelt F, Suresh Babu MP, Szelenyi A, Rapp M, Sabel M. Establishment of Different Intraoperative Monitoring and Mapping Techniques and Their Impact on Survival, Extent of Resection, and Clinical Outcome in Patients with High-Grade Gliomas-A Series of 631 Patients in 14 Years. Cancers (Basel). Feb 25 2024;16(5)doi:10.3390/cancers16050926
- Sabel M, Staub-Bartelt F, Todter J, et al. In Reply to the Letter to the Editor Regarding „Improved Availability of Fluorescence-Guided Surgery of Malignant Brain Tumors: A Headlamp-Loupe System Combined With Generic 5-Aminolevulinic Acid Replaces the Microscope-A Monocentric Feasibility Study“. World Neurosurg. Dec 2025;204:124571. doi:10.1016/j.wneu.2025.124571
- Jansen NL, Graute V, Armbruster L, et al. MRI-suspected low-grade glioma: is there a need to perform dynamic FET PET? Eur J Nucl Med Mol Imaging. Jun 2012;39(6):1021-9. doi:10.1007/s00259-012-2109-9
- Jansen NL, Suchorska B, Wenter V, et al. Dynamic 18F-FET PET in newly diagnosed astrocytic low-grade glioma identifies high-risk patients. J Nucl Med. Feb 2014;55(2):198-203. doi:10.2967/jnumed.113.122333
- Langen KJ, Stoffels G, Filss CP, et al. Borderline Findings in O-(2-[(18)F]-Fluoroethyl)-l-Tyrosine PET of Patients with Suspected Glioma Relapse: Role in Clinical Practice. J Nucl Med. Feb 3 2025;66(2):187-193. doi:10.2967/jnumed.124.268768
- Rapp M, Ozcan Z, Steiger HJ, Wernet P, Sabel MC, Sorg RV. Cellular immunity of patients with malignant glioma: prerequisites for dendritic cell vaccination immunotherapy. J Neurosurg. Jul 2006;105(1):41-50. doi:10.3171/jns.2006.105.1.41
- Staub-Bartelt F, Hofmann BB, Rapp M, Hanggi D, Kamp MA, Sabel M. Direct Cortical Stimulation in Neurosurgical Emergencies: Single-Center Experience in 2 Patients. World Neurosurg. Jun 2021;150:147-152. doi:10.1016/j.wneu.2021.03.118
- Staub-Bartelt F, Obermayr S, Sabel M, Rapp M. Influence of neuropathological diagnosis on psychooncological distress in neurooncological patients – a retrospective cross-sectional analysis. Front Oncol. 2024;14:1457017. doi:10.3389/fonc.2024.1457017
- Staub-Bartelt F, Steinmann J, Radtke O, Hanggi D, Sabel M, Rapp M. Impact of COVID-19 Epidemic on Psycho-Oncological Distress in Neuro-Oncological Patients. Curr Oncol. Dec 26 2022;30(1):358-369. doi:10.3390/curroncol30010029
- Staub-Bartelt F, Steinmann J, Wienand M, Sabel M, Rapp M. Increased Distress in Neurooncological Patients, a Monocentric Longitudinal Study: When to Screen Which Patient? Diseases. Sep 16 2024;12(9)doi:10.3390/diseases12090217
- Kamp MA, Santacroce A, Zella S, et al. Is it a glioblastoma? In dubio pro 5-ALA! Acta Neurochir (Wien). Jul 2012;154(7):1269-73. doi:10.1007/s00701-012-1369-2